Hình 1: Hai nhà khoa học Katalin Karikó và Drew Weissman
(Nguồn: Sưu tầm)
Kết quả nghiên cứu của hai nhà khoa học vừa đoạt giải Nobel có ý nghĩa quan trọng trong việc phát triển vắc-xin mRNA chống lại COVID-19 trong đại dịch bắt đầu vào đầu năm 2020. Những phát hiện mang tính đột phá này đã thay đổi căn bản hiểu biết của chúng ta về cách mRNA tương tác với hệ thống miễn dịch của cơ thể, đóng góp lớn vào tốc độ phát triển vắc-xin vô tiền khoáng hậu trước dịch bệnh đe dọa lớn nhất đối với sức khỏe con người trong thời hiện đại.
Trước đó, năm 1951, nhà khoa học Max Theiler (1899-1972) cũng từng được trao giải Nobel về Sinh lý học hoặc Y học vì đã phát hiện virus gây sốt vàng da và phát hiện vắc-xin phòng bệnh.
Hành trình được trao giải Nobel cũng vô cũng khó khăn và vất vả cho các nhà khoa học nghiên cứu sinh lý học hoặc y học. Tiến sĩ Theiler, lần đầu tiên được đề cử giải Nobel về sinh lý học hoặc y học vào năm 1937, nhưng mãi đến 14 năm sau (1951) ông mới được trao giải Nobel, trong khi đó hai nhà khoa học Katalin Karikó và Drew Weissman được trao giải Nobel sau 18 năm (2005-2023) từ khi phát hiện lần đầu và công bố kết quả nghiên cứu về mRNA.
Trong tế bào của chúng ta, thông tin di truyền được mã hóa trong DNA được chuyển sang RNA thông tin (mRNA), được sử dụng làm khuôn mẫu để sản xuất protein. Trong những năm 1980, các phương pháp hiệu quả để sản xuất mRNA mà không cần nuôi cấy tế bào đã được giới thiệu, được gọi là phiên mã in vitro. Bước quyết định này đã đẩy nhanh sự phát triển các ứng dụng sinh học phân tử trong một số lĩnh vực. Ý tưởng sử dụng công nghệ mRNA cho mục đích điều trị và vắc-xin cũng được triển khai nhưng vẫn còn nhiều rào cản phía trước. Phiên mã in vitro mRNA được coi là không ổn định và khó phân phối, đòi hỏi phải phát triển các hệ thống lipid vận chuyển phức tạp để bao bọc mRNA. Hơn nữa, mRNA phiên mã in vitro gây gia tăng phản ứng viêm. Do đó, sự thuận lợi cho phát triển công nghệ mRNA cho mục đích lâm sàng ban đầu bị hạn chế.
Những trở ngại này không làm nản lòng nhà hóa sinh người Hungary Katalin Karikó, người đã cống hiến hết mình cho việc phát triển các phương pháp sử dụng mRNA để trị liệu. Một đồng nghiệp mới của Karikó tại trường đại học của cô là nhà miễn dịch học Drew Weissman. Ông quan tâm đến các tế bào đuôi gai (dendritic cells), có chức năng quan trọng trong việc giám sát miễn dịch và kích hoạt các phản ứng miễn dịch do vắc-xin gây ra. Được thúc đẩy bởi những ý tưởng mới, sự hợp tác hiệu quả giữa hai bên đã sớm bắt đầu, tập trung vào cách các loại RNA khác nhau tương tác với hệ thống miễn dịch.
ĐỘT PHÁ
Karikó và Weissman nhận thấy rằng các tế bào đuôi gai nhận ra mRNA được phiên mã in vitro là một chất lạ, dẫn đến việc chúng kích hoạt và giải phóng các phân tử tín hiệu viêm. Họ tự hỏi tại sao mRNA được phiên mã in vitro lại được coi là ngoại lai trong khi mRNA từ tế bào động vật có vú lại không gây ra phản ứng tương tự. Karikó và Weissman nhận ra rằng một số đặc tính quan trọng giúp phân biệt các loại mRNA khác nhau.
RNA chứa bốn bazơ, viết tắt là A, U, G và C, tương ứng với các chữ cái của mã di truyền là A, T, G và C trong DNA. Karikó và Weissman biết rằng các bazơ trong RNA từ tế bào động vật có vú thường xuyên bị biến đổi về mặt hóa học, trong khi mRNA được phiên mã in vitro thì không. Họ tự hỏi liệu sự vắng mặt của các bazơ bị thay đổi trong RNA phiên mã in vitro có thể giải thích phản ứng viêm không mong muốn hay không. Để nghiên cứu điều này, họ đã tạo ra các biến thể khác nhau của mRNA, mỗi biến thể có những thay đổi hóa học riêng biệt trong các bazơ mà họ chuyển đến các tế bào đuôi gai. Kết quả thật đáng ngạc nhiên: Phản ứng viêm gần như bị loại bỏ khi các biến đổi bazơ được đưa vào mRNA. Đây là một sự thay đổi về mô hình trong hiểu biết của chúng ta về cách tế bào nhận biết và phản ứng với các dạng mRNA khác nhau. Karikó và Weissman ngay lập tức hiểu rằng khám phá của họ có ý nghĩa sâu sắc đối với việc sử dụng mRNA làm liệu pháp. Những kết quả quan trọng này được công bố vào năm 2005, mười lăm năm trước đại dịch COVID-19.
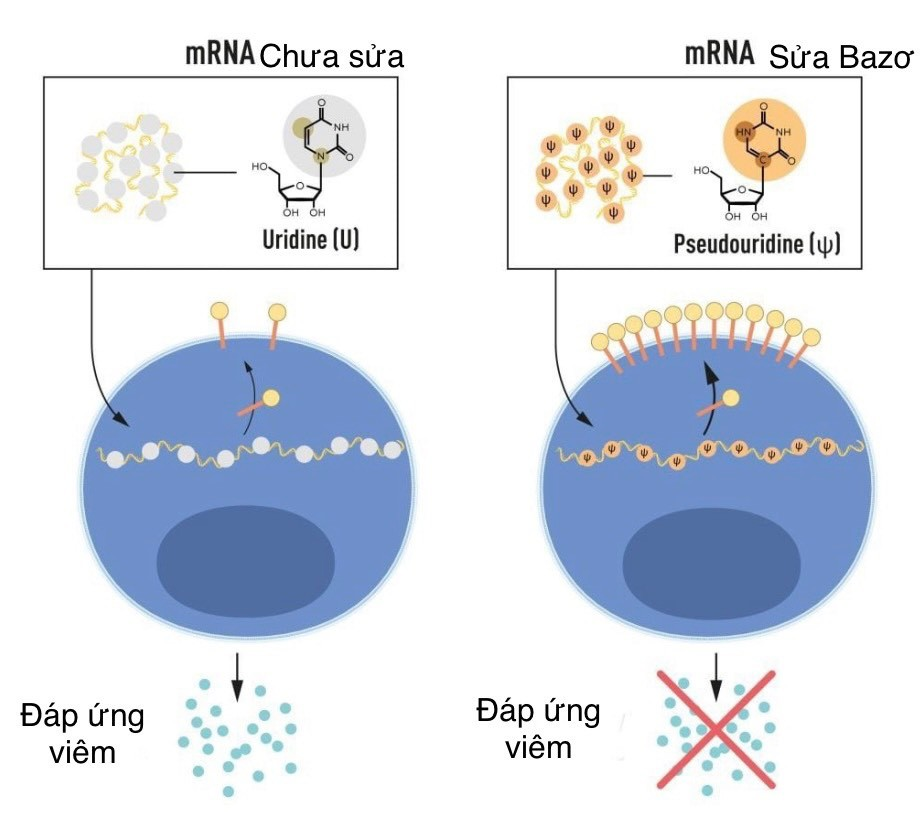
Hình 2: mRNA biến đổi bazơ có thể được sử dụng để ngăn chặn sự kích hoạt các phản ứng viêm
Trong các nghiên cứu sâu hơn được công bố vào năm 2008 và 2010, Karikó và Weissman đã chỉ ra rằng việc cung cấp mRNA được tạo ra bằng các sửa đổi bazơ đã làm tăng đáng kể việc sản xuất protein so với mRNA không được sửa đổi. Hiệu quả này là do sự giảm kích hoạt của một loại enzyme điều chỉnh quá trình sản xuất protein. Thông qua những khám phá của họ rằng việc sửa đổi cơ sở vừa làm giảm phản ứng viêm vừa tăng sản xuất protein, Karikó và Weissman đã loại bỏ những trở ngại quan trọng trên con đường ứng dụng lâm sàng của mRNA.
Sự quan tâm đến công nghệ mRNA bắt đầu tăng lên và vào năm 2010, một số công ty đã nỗ lực phát triển phương pháp này. Các loại vắc-xin chống vi-rút Zika và MERS-CoV đã được nghiên cứu, vắc-xin chống MERS-CoV có liên quan chặt chẽ với SARS-CoV-2. Sau khi đại dịch COVID-19 bùng phát, hai loại vắc- xin mRNA biến đổi bazơ mã hóa protein bề mặt SARS-CoV-2 đã được phát triển với tốc độ kỷ lục. Tác dụng bảo vệ đã được báo cáo là khoảng 95% và cả hai loại vắc-xin đều đã được phê duyệt vào tháng 12 năm 2020.
Tính linh hoạt và tốc độ ấn tượng mà vắc-xin mRNA có thể được phát triển đã mở đường cho việc sử dụng nền tảng mới cho cả vắc-xin chống lại các bệnh truyền nhiễm khác. Trong tương lai, công nghệ này cũng có thể được sử dụng để cung cấp các protein trị liệu và điều trị một số loại ung thư.
Một số loại vắc-xin khác chống lại SARS-CoV-2, dựa trên các phương pháp khác nhau, cũng nhanh chóng được giới thiệu và tổng cộng hơn 13 tỷ liều vắc-xin COVID-19 đã được tiêm trên toàn cầu. Vắc-xin đã cứu sống hàng triệu người và ngăn ngừa bệnh tật nghiêm trọng ở nhiều người khác, cho phép xã hội mở cửa trở lại điều kiện bình thường. Thông qua những khám phá cơ bản về tầm quan trọng của việc sửa đổi cơ sở trong mRNA, những người đoạt giải Nobel năm nay đã góp phần quan trọng vào sự phát triển mang tính biến đổi này trong một trong những cuộc khủng hoảng sức khỏe lớn nhất của thời đại chúng ta.
Mặc dù Max Theiler di cư sang Mỹ vào năm 1923 và ở đó đến hết đời nhưng ông chưa bao giờ nộp đơn xin quốc tịch Mỹ. Khi được hỏi ông sẽ làm gì với số tiền thưởng (khoảng 32.000 USD vào năm 1951) đi kèm với giải Nobel, Theiler trả lời rằng ông sẽ mua một thùng rượu Scotch và xem đội Brooklyn Dodgers chơi bóng chày.
Karikó, 68 tuổi, là người phụ nữ thứ 13 đoạt giải Nobel y học. Karikó và Weissman, 64 tuổi, tình cờ gặp nhau vào những năm 1990 khi đang sao chép các tài liệu nghiên cứu.
Nhân dịp trao giải Nobel về sinh lý học hoặc y học năm 2023, chúng ta lại thấy những người hùng xuất hiện cứu cả thế giới không phải là các Iron Man trong các phim hành động Mỹ mà đôi khi lại ở trong vỏ bọc khác lạ: hài hước và bình dị.
TÀI LIỆU THAM KHẢO:
1. Siang Yong Tan, Kate Pettigrew (2017), “Max Theiler (1899-1972): Creator of the yellow fever vaccine”, Singapore Med J, 58(4),223-224.
2. The Nobel Prize 2023
(https://www.nobelprize.org/uploads/2023/10/press-medicineprize2023-3.pdf)